요약
암세포를 터뜨려 죽이는 나노버블로 면역 물질의 손상을 막는 연구가 등장했습니다. 초음파 조사 시 종양세포가 스스로 세포막 붕괴를 일으켜 죽는 네크롭토시스를 물리적으로 유발할 수 있는 나노버블을 만든 겁니다. 이 연구는 네크롭토시스를 통한 항암 면역치료 연구의 실마리를 제시했습니다.
물리적으로 암세포의 사멸을 유도해 암세포에 대한 체내 대항력을 증폭시킬 수 있는 고분자 나노버블이 소개됐습니다. 성균관대학교 박재형 교수 연구팀이 초음파를 쬐면 기포가 나오는 나노버블로 암 세포막 파열을 유발, 네크롭토시스 유사 세포사멸을 유도했다고 밝혔습니다. 해당 연구는 <Advanced Materials>에 게재됐습니다.

'네크롭토시스' 이용하자
세포막을 붕괴시켜 스스로 사멸하는 괴사의 일종인 네크롭토시스(necroptosis)는 카스파아제 등 분해효소가 관여하는 자멸사(apoptosis)와 달리 단백질 분해나 산화 등이 일어나지 않아 암 표지자나 면역유발물질의 손상을 최소화할 수 있습니다.
죽어가는 암세포를 면역 반응을 활성화시킬 자극제로 이용한다면 면역관문억제제의 반응성을 높이는 한편 남아 있거나 전이되었을지 모를 암세포에 대한 체내 면역을 유지하는 데 유리합니다. 하지만 대부분의 암에서 네크롭토시스를 유발하는 단백질(RIPK3) 발현양이 낮아 이를 이용한 치료제 개발에 난항을 겪고 있었습니다.
- 면역관문억제제
T세포가 암세포를 공격대상으로 인지하지 못하게 하는 암세포의 면역회피신호를 억제하는 항체
- RIPK3
네크롭토시스 과정에서 최종적으로 세포막 붕괴를 유도하는 단백질의 활성을 조절하는 인산화효소
물리적 자극으로 네크롭토시스 유발
이에 단백질이 아닌 물리적 자극으로 네크롭토시스를 유발하고자 했습니다. 연구팀은 네크롭토시스가 세포막 파열을 수반하는 데 착안해 기포를 이용해 암세포를 터뜨리는 고분자를 설계했습니다. 자가조립형 고분자에 액체 상태의 과불화펜탄을 탑재해 초음파를 쬐어주면 과불화펜탄이 기체로 변하면서 부피가 팽창, 세포막의 붕괴를 유도하는 원리입니다.
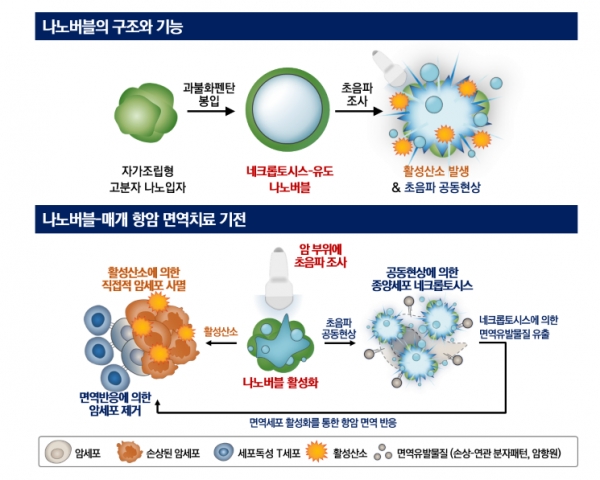
연구팀은 RIPK3 단백질 발현 유무와 상관없이 초음파 조사 시 나노버블에 의해 암세포의 구조가 붕괴되는 것을 공초점현미경을 통해 관찰했습니다. 실제 대장암 세포에 나노버블을 처리하면 활성산소를 처리한 경우와 달리 세포손상에 대응하는 면역유발물질(HMGB1)이 산화되지 않고 다량 방출, 면역세포인 수지상세포의 성숙도를 월등히 높이는 것을 확인했습니다.
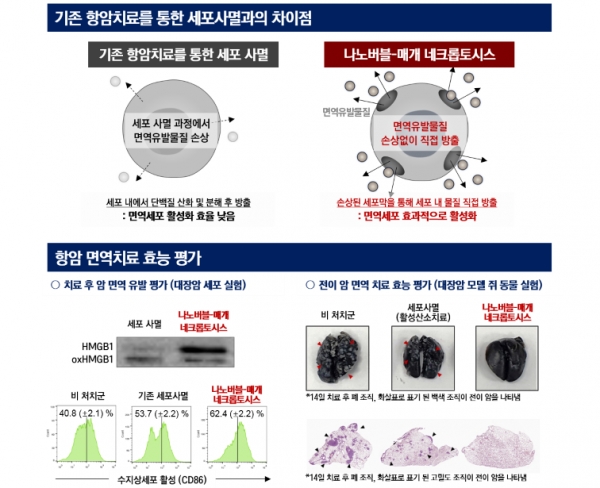
나아가 폐로 암이 전이된 생쥐 모델에 면역관문억제제(PD-L1 항체)와 함께 나노버블을 병용투여한 결과 억제제 단독투여시 보다 종양의 무게가 97% 수준의 감소율을 나타내는 등 반응성이 향상됐습니다. 종양 내 암세포를 공격하는 면역세포(CD8+ T세포)가 월등히 늘어났고 잔존 암과 전이암의 성장이 확연히 억제되는 것을 통해 나노버블에 의한 네크롭토시스 유도가 결과적으로 면역체계 활성화를 이끌었음을 확인했습니다.
항암 면역치료 연구 실마리 제시
이 연구는 네크롭토시스를 통한 항암 면역치료 연구의 실마리를 제시했습니다. 면역원성 세포사멸을 유도하기 위해 저분자 화합물 전달 중심의 기존 연구 패러다임에서 벗어나 암 조직 선택적 기포발생을 통해 세포 팽창을 유발하여 면역세포의 활성을 극대화하는 전략을 제시했습니다.
특정 단백질의 발현 양상에 따라 치료 효율이 달라지는 종래 네크롭토시스 유발제제들과 달리 물리적으로 네크롭토시스를 유도하기에 암 종에 국한되지 않고 응용될 수 있을 것으로 기대됩니다. 또한 초음파 감응성을 도입, 세포사멸의 시·공간적 제어가 가능해 부작용을 줄일 수 있을 것으로 기대됩니다.
##참고자료##

