국내 연구진이 루게릭병 독성 단백질 생성을 억제하는 신경세포보호 유전자를 새롭게 발견했습니다. 루게릭병은 독성 단백질이 세포내에서 쌓여 신경세포가 죽는 대표적 퇴행성 뇌질환인데요.
UNIST 생명과학과 임정훈 교수팀은 루게릭병, 전측두엽 치매 같은 퇴행성 뇌질환을 억제하는 유전자인 ‘ZNF598’을 발견하고 신경세포 보호의 새로운 분자생물학적 원리를 규명했다고 30일 밝혔습니다. 이 유전자는 루게릭병 환자 신경세포 내 독성 단백질 번역 산물을 제거해 세포사멸을 억제하는 것으로 나타났습니다. 이번 연구 결과는 효과적인 퇴행성 뇌질환 조기 진단과 근본적인 뇌질환 치료제 개발의 새로운 열쇠가 될 전망입니다.
임 교수 연구팀은 ZNF598 유전자를 활성화해 루게릭병 환자 유래 신경세포의 사멸을 억제했습니다. ZNF598은 단백질 번역 품질 관리 경로를 통해 이러한 기능을 수행했는데요. 단백질 번역 품질 관리는 비정상적으로 생성되고 있는 번역 중간산물을 인지해 이를 분해하는 과정입니다. 단백질 번역을 담당하는 리보솜이 비정상적인 번역 과정 도중에 멈추게 되면(리보솜 정체) 단백질 번역 품질관리 경로가 활성화되고, 번역 산물이 리보솜에서 분리돼 분해됩니다. 연구결과에 따르면 루게릭병의 독성단백질이 리보솜 정체 현상을 유발합니다.
한편, 번역은 mRNA가 가지고 있는 유전 암호로부터 단백질의 기본구조가 합성되는 과정입니다. 리보솜이 mRNA의 염기서열에 해당하는 각각의 아미노산을 연결해 단백질 기본 구조인 번역산물을 만듭니다. 이 과정에서 잘못된 유전 정보가 독성 단백질로 번역되면 신경세포가 죽는 루게릭병과 같은 퇴행성 뇌질환이 발생하는 것으로 알려져 있습니다.
제1저자로 연구에 참여한 박주민 연구원(UNIST 생명과학과 석박사 통합과정)은 “루게릭병 독성단백질의 세포 독성을 제어하는 유전자를 찾는 과정에서 ZNF598 유전자가 신경세포 퇴화를 억제한다는 단서를 발견하고, 이를 다양한 유전자 편집과 제어 모델을 활용해 검증했다”며 “특히 자체 개발한 기술을 통해 독성 단백질이 번역될 때 리보솜 정체 현상 일어난다는 사실을 밝혀냈다”고 설명했습니다.
임정훈 교수는 “루게릭병 환자의 유도만능줄기세포에서 분화한 운동신경 세포에서는 ZNF598와 같이 단백질 번역 품질 관리에 관여하는 주요 유전자들이 비정상적으로 발현되며, 결과적으로 단백질 번역 품질 관리가 제대로 일어나지 않는 것을 확인했다”고 설명했습니다. 임 교수는 이어 “단백질 번역 품질 관리의 기능 분석과 제어 기술이 루게릭병, 전측두엽 치매와 같은 관련 질환의 예측과 진단, 치료 기술 개발에 있어 새로운 돌파구를 마련해줄 것“이라고 기대했습니다.
이번 연구 결과는 생명과학 분야 학술지 ‘핵산연구(Nucleic acid research)저널’의 9월 22일자 온라인 판에 게재되었다. 이번 연구는 서경배과학재단, 한국연구재단의 중견연구지원사업, 선도연구센터지원사업, 바이오의료기술개발사업을 통해 이루어졌다.
논문명: ZNF598 co-translationally titrates poly(GR) protein implicated in the pathogenesis of C9ORF72-associated ALS/FTD
#연구 결과 개요
1. 연구배경
리보솜에 의한 단백질 번역 과정은 DNA에 저장된 유전 정보가 RNA로 전사되어 생물학적 기능을 가진 단백질로 합성되기까지 세포의 필수적인 작용 가운데 하나이다. 최근에는 번역 과정에서의 기능 장애가 퇴행성 뇌질환의 중요한 병리학적 원인으로 새롭게 대두되고 있으나, 어떠한 분자생물학적 기전을 통해 퇴행성 뇌질환을 초래하는지에 대한 이해가 부족한 실정이다. 본 연구팀은 루게릭병 환자의 유도만능줄기세포로부터 분화한 운동신경 세포, 인간 신경아세포종, 초파리 생체모델 등을 활용하여 루게릭병 독성 단백질의 번역 과정에서 이를 조절하는 단백질 번역 품질 관리 유전자들의 새로운 기능을 발견하고, 신경세포 보호 작용을 검증하였다.
2. 연구내용
RNA로 전사된 유전 암호를 해독하여 단백질로 번역하는 기능을 담당하는 리보솜은 다양한 기능을 가지고 있는 여러 단백질들과 결합하여 작용한다. 리보솜 결합 단백질 가운데 하나인 ZNF598은 단백질 번역 품질 관리 기능을 담당하며, 번역 중이던 리보솜이 RNA 손상이나 비정상적인 유전 정보에 의해 멈춰 정체가 일어나고 뒤따르던 리보솜이 충돌하게 되면 이를 인지하여 특정 리보솜 단백질의 유비퀴틴화를 통해 리보솜 분리를 촉진한다. 이후 일련의 단백질 번역 품질 관리 인자들에 의해 번역 중이던 RNA와 비정상적인 단백질 번역 산물의 분해가 일어나게 되며, 이를 통해 세포 내 단백질 항상성이 유지되게 된다.
본 연구팀은 루게릭병 독성단백질로 알려져 있는 poly(GR) 단백질의 세포 독성을 제어하는 새로운 유전자를 발굴하기 위해 형질전환 초파리를 활용한 유전자 탐색을 수행하였다. 이를 통해 ZNF598을 포함하여 단백질 번역 품질 관리에 작용하는 여러 유전자들이 poly(GR) 단백질에 의한 신경퇴화를 억제한다는 단서를 찾고, 이를 루게릭병 환자의 유도만능줄기세포에서 분화한 운동신경 세포와 신경아세포종 주에서 검증하였다.
신경아세포종 내 단백질 번역 활성 리포터 유전자 발현을 통해 poly(GR) 단백질의 번역 과정에서 실제로 리보솜 정체가 일어나는 것을 확인하고, 면역침강법과 자당 밀도 구배 원심 분리를 이용하여 poly(GR) 단백질 번역 산물이 리보솜 및 단백질 번역 품질 관리 조절 단백질(ZNF598, NEMF, LTN1)들과 생화학적 상호작용을 통해 단백질 복합체를 형성하는 것을 관찰하였다. 또한 크리스퍼 유전자 가위를 이용한 유전자 편집 세포주를 활용하여, ZNF598, NEMF, LTN1 유전자의 단백질 번역 품질 관리 기능이 poly(GR) 단백질의 비정상적인 번역 과정에서 발생하는 번역 산물의 유비퀴틴화를 통해 poly(GR) 단백질 분해를 촉진한다는 사실을 규명하였다.
루게릭병 환자의 전장유전체 분석 데이터(유전체의 염기서열 전체를 분석하는 방법)로부터 ZNF598 유전자의 희귀한 돌연변이를 발견하였으며, 면역형광염색, 유세포 분석, 단백질 분석 기법 등을 통해 해당 돌연변이에 의해 ZNF598 단백질의 번역 품질 관리 기능이 상실하게 된다는 것을 확인하였다.
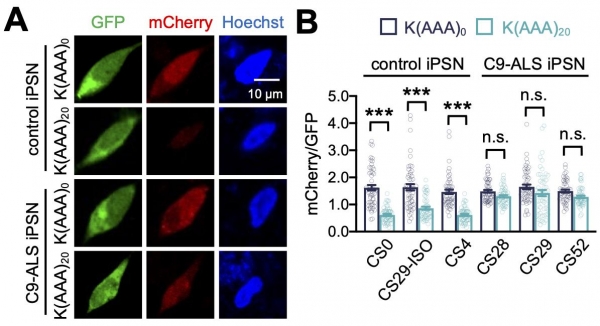
퇴행성 뇌질환 발병에 있어 이러한 단백질 번역 품질 관리 기능의 병리학적 중요성을 검증하기 위해, 루게릭병 환자의 유도만능줄기세포로부터 분화한 운동신경 세포 모델을 활용하였다. 정상 신경세포와의 유전자 발현 비교 분석을 통해, 루게릭병 환자의 운동신경 세포에서 단백질 번역 품질 관리 유전자들의 발현이 변화하며 특히 ZNF598 단백질 발현이 감소되어 있는 것을 확인하였다. 또한, 단백질 번역 품질 관리 활성을 측정할 수 있는 형광 리포터 유전자를 통해 루게릭병 환자유래 신경세포 내 단백질 번역 품질 관리의 기능 장애를 확인하였다.
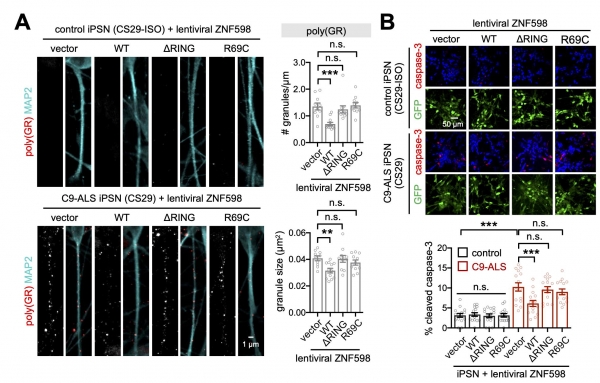
마지막으로 연구팀은 재조합 렌티 바이러스를 이용하여 루게릭병 환자유래 신경세포 내에 ZNF598 단백질을 과발현하여 단백질 번역 품질 관리 기능을 활성화 할 경우 루게릭병 환자 신경세포에서 특이적으로 관찰되는 poly(GR) 독성 단백질의 발현이 억제되는 것을 관찰하였다. 이와 함께 세포사멸 마커인 caspase-3 발현 분석을 통해
ZNF598 과발현이 루게릭병 환자유래 신경세포에서 특이적으로 나타나는 세포사멸 활성화를 억제한다는 것을 검증하였다.
3. 기대효과
본 연구를 통해 루게릭병 환자유래 신경세포의 단백질 번역 품질 관리 기능 장애를 확인하고, 형질전환 바이러스를 이용한 ZNF598 유전자 기능 활성화를 통해 루게릭병 독성단백질 제거와 신경세포 사멸 억제를 검증하였다. 새롭게 확립된 루게릭병, 전측두엽 치매 등 퇴행성 뇌질환의 분자생물학적 발병 원리에 관한 기반 지식과 원천 기술을 바탕으로 단백질 번역 품질 관리 기능과 관련된 분자 표적을 통해 퇴행성 뇌질환의 조기진단 및 치료기술 개발에 기여할 수 있을 것으로 전망된다.
#용어설명
1. 퇴행성 뇌질환
중추신경계의 특정 신경세포가 비가역적으로 퇴화하면서 나타나는 여러 특징적인 증상을 수반하는 신경질환이다. 알츠하이머 치매, 파킨슨병, 헌팅턴병 등이 대표적인 예이다. 메이저리그 뉴욕 양키스의 유명 내야수였던 루 게릭(Lou Gehrig)에게 발병하면서 루게릭병으로도 불리게 된 근위축성 측색 경화증(ALS, amyotrophic lateral sclerosis)의 경우, 운동신경 세포의 기능이 손상되면서 근육쇠약과 호흡장애 등으로 대부분의 발병 환자가 수년 내에 사망한다.
2. 리보솜 정체
RNA에 결합한 리보솜이 RNA 염기서열의 유전암호 해독을 통해 단백질을 합성하는 과정에서 특정한 염기서열, RNA 이차구조, RNA 손상, 아미노산-tRNA 결핍 등의 원인에 의해 RNA 중간에 멈춰서는 현상이다. 정체된 선행 리보솜이 뒤따라오는 리보솜과 충돌할 경우 2개의 리보솜이 다이솜(di-some)이라고 불리는 특이적인 3차 구조를 형성하게 되는데, 이를 리보솜과 결합하고 있는 ZNF598 단백질이 인지하여 단백질 번역 품질 관리 기능을 활성화하는 것으로 알려져 있다.
3. 단백질 번역 품질 관리
리보솜 정체를 세포 내 비정상적인 단백질 번역 과정으로 인지하여 이를 해소하고, 관련 부산물이 정상적인 세포 생리작용을 방해하지 않도록 분해하는 기능을 담당한다. 1) 리보솜 정체 인지, 2) 정체된 리보솜의 분리와 재활용, 3) 비정상적인 단백질 번역 과정에서 만들어진 번역 산물(번역 중간체와 RNA)의 제거 순으로 작용한다. 이때 ZNF598과 LTN1은 정체된 리보솜 단백질과 단백질 번역 산물에 유비퀴틴이라고 불리는 작은 조절 단백질을 부착하는 효소로 작용하여 리보솜의 분리와 프로테아좀에 의한 단백질 분해를 유도한다고 알려져 있다.

