
서울대학교 약대 이정원 교수 연구팀이 혈중 포도당 항상성을 조절하는 새로운 메커니즘을 제시했습니다. 간유래 TM4SF5-탑재 소포체의
혈중 포도당 항상성 유지 기능을 규명한 겁니다.
간세포와 조직 유래 소포체를 분리
이 교수 연구팀은 세포 혹은 생쥐 실험동물 모델에서 간세포 유래 소포체(엑소좀)을 분리해 분석하는 기술을 개발했습니다. 포도당 수준이 다른 환경에서 간세포 유래 소포체를 분리, 분석한 결과 소포체의 크기가 달라짐을 밝힌 거죠. TM4SF5 막단백질이 발현하는 간상피세포 혹은 실험동물의 간 조직에서 분리된 소포체가 작아지고, 다른 세포나 장기를 표적할 수 있는 단백질들이 추가적으로 탑재될 수 있음을 확인했습니다. 간세포 혹은 간 조직으로부터 분리한 TM4SF5-탑재된 소포체에 형광 표지를 한 후 마우스에 주입하여 소포체의 생체 내 장기들로의 이동을 추적했습니다.
이러한 성과는 혈액 내 존재하는 소포체들 가운데 간세포 유래 소포체만을 분리할 수 있게 만들었습니다. 또한 간세포에서 분비되는 소포체를 추적하여 간과 다른 장기 및 기관 사이의 상호작용을 밝혀냈습니다. TM4SF5-탑재 소포체를 통한 간-갈색지방조직 사이의 상호작용이 혈중 포도당 항상성 유지에 기여한다는 점도 확인했습니다. 연구팀은 간상피세포 외부의 포도당 농도 향상에 따른 간상피세포로부터 유래된 TM4SF5-탑재 소포체의 분비가 유발된다는 점도 발견했습니다.
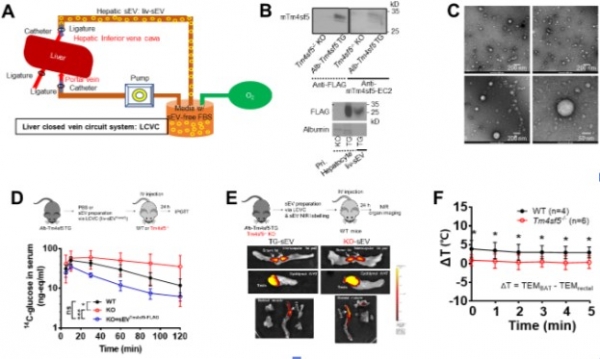
(B) Liver-closed vein circuit system을 이용하여 생쥐의 간세포로부터 얻은 소포체에 존재하는
Tm4sf5의 탑재를 확인하는 단백질 면역블랏.
(C) Liver-closed vein circuit system을 이용하여 생쥐의 간세포로부터 얻은 소포체를 전자현미경으로 확인한 이미지
(D) Tm4sf5를 과발현하도록 제작한 유전자변형동물(Alb-Tm4sf5 TG)로부터 얻은 간유래 소포체를 정상(WT) 혹은 Tm4sf5 유전자 결여 동물(KO)에게 정맥에 주사하고 난 후, 포도당을 체내에 투여하고 시간별로 혈액을 채취하여 혈중 포도당의 농도를 측정하여 혈당의 변화를 추적한 실험. KO 마우스보다 WT 마우스에서 시간에 따른 혈당의 감소가 돋보임. 더욱이, TG 마우스의 간유래 소포체를 주사한 WT 마우스의 경우, 혈당의 감소가 더욱더 두드러지게 감소함.
(E) Alb-Tm4sf5 TG 혹은 Tm4sf5 유전자 결여 KO 마우스로부터 liver-closed vein circuit system을 이용하여 얻은 소포체에 근적외선 형광염료를 처리하여 표식한 후, 정상 마우스에 정맥에 주사하여 각 장기에 소포체의 존재 여부를 생체이미징 기법을 통해 확인한 그림. TG 마우스 간유래 소포체가 KO 마우스 간유래 소포체보다 갈색지방조직으로의 이동이 좀 더 강하게 보임.
(F) 정상(WT) 및 Tm4sf5 유전자 결여(KO) 마우스를 4℃에 3시간 방치 후, 실온으로 옮긴 후 1분마다 5번을 각 동물의 체온을 측정한 결과임. 각 마우스의 체온은 항문 체온과 등부위 갈색지방조직에의 체온을 동시에 측정하여 그 차잇값(= 갈색지방조직 체온-항문 체온)을 그래프로 표현한 것임. 즉, Tm4sf5 유전자가 결여된 마우스에는 간유래-Tm4sf5를 포함하는 소포체의 역할이 없는 경우로서, Tm4sf5-기반 소포체가 존재하는 정상 마우스에 대비하여 체온이 낮음. 이는 Tm4sf5가 탑재된 소포체가 정상 마우스에서는 간으로부터 분비되어 갈색지방조직으로 이동하여 갈색지방세포의 혈중 포도당 흡수 및 소모를 통한 열 생성의 기전으로 혈당 조절 및 체온 조절이 되는 것으로 추정 가능하였음.
출처: 서울대학교
혈중 인슐린의 수준과는 별개로, 간상피세포에 발현되는 TM4SF5는 포도당 수송체 type 1(GLUT1)과의 결합을 통해, 간상피세포 내부로의 포도당 흡수를 향상시켰는데요. 한편, 간상피세포에서 유래된 TM4SF5가 탑재된 소포체의 분비가 유발된다는 점을 파악했습니다.
간상피세포에서 유래된 TM4SF5가 탑재된 소포체는 혈액을 통해 갈색지방조직으로 전달된다는 점도 포착했습니다. 소포체를 통해 갈색지방세포로 전해진 단백질 가운데 TM4SF5가 갈색지방세포의 세포막에 위치하여 포도당 수송체 type 4(GLUT4)와의 결합을 통해 세포 내부로 포도당 유입을 촉진함을 확인했습니다. 이는 인슐린의 작용과는 별도의 현상으로 추정됩니다.
TM4SF5가 탑재된 소포체의 이동 후, 갈색지방세포에서 열 발생을 통해 포도당을 소모함을 밝혔습니다. 특히 TM4SF5-탑재 소포체의 갈색지방조직으로의 이동에 따른 동물의 체온 조절에 의미가 있음을 확인한 겁니다. TM4SF5-탑재 소포체의 이동을 통한 간-갈색지방조직의 상호작용으로 인슐린의 작용과는 별도로 혈중 포도당 농도가 적절히 조절될 수 있다는 점도 알아냈습니다. TM4SF5-탑재 소포체를 통한 혈중 포도당 항상성 및 건강한 생체 기능 유지와의 상관성도 밝혀냈습니다.
TM4SF5 유전자 결여 및 과발현 유전자변형동물의 (2년 이상) 장기 사육을 통한 체중 및 생존율의 조사 분석을 수행했는데요. TM4SF5-탑재 소포체의 이동을 통한 간-갈색지방조직의 상호작용에 따라, 실험동물들의 신진대사, 체중 조절, 및 생존율(수명) 등의 건강이 좋아질 수 있음이 연계되어 추정됐습니다.
포도당 대사의 항상성 조절 새 기전
이러한 연구성과는, 인슐린의 작용과는 별도로, TM4SF5-탑재 소포체 기반의 포도당 대사의 항상성을 조절할 수 있는 새로운 기전을 제시하는 것입니다. 또한, TM4SF5-탑재된 간유래 소포체 엔지니어링을 통해 대사성 질환을 완화하는 예방 및 치료법을 개발할 수 있을 것으로 기대됩니다.
본 연구 결과는 2022년 9월 5일 세포생물학 관련 권위지인 'Journal of Extracellular Vesicles' 온라인판에 게재됐습니다.
출처: Impact factor, 17.335, 2021 JCR

